Tekorten
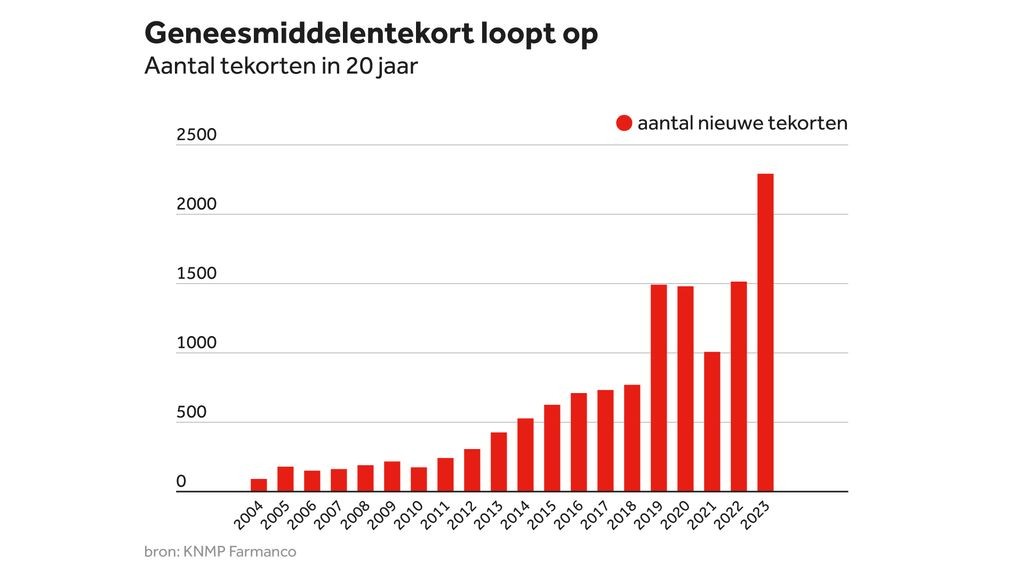
In Nederland zijn de geneesmiddeltekorten nog nooit zo groot geweest als nu. Volgens de KNMP zijn in 2024 meer dan 4,5 miljoen mensen getroffen door deze tekorten. Gemiddeld is in elke apotheek één fte uitsluitend bezig met het oplossen van geneesmiddeltekorten en het vinden van een passende oplossing voor de patiënt.
Het aantal tekorten bereikte in 2023 een piek: meer dan 2.000 geneesmiddelen waren (tijdelijk) niet leverbaar. Dit heeft grote gevolgen voor patiënten, apotheken, ziekenhuizen en de gehele zorgketen.
Over ons
Zorg zonder grenzen, voor elke patiënt, elk geneesmiddel, altijd beschikbaar.
Om patiënten de juiste zorg te bieden en apotheken en ziekenhuizen te ontzorgen bij het oplossen van geneesmiddeltekorten, ondersteunen wij via import. Wij importeren geneesmiddelen die in Nederland (tijdelijk) niet beschikbaar zijn en bieden daarmee een oplossing voor de gehele zorgketen.
Met ruime ervaring in de import van geneesmiddelen en een flexibele werkwijze, spelen wij snel in op de behoeften van de markt. We werken uitsluitend met geautoriseerde partners en volledig volgens de GDP-richtlijnen, om de kwaliteit en veiligheid van de geneesmiddelen te waarborgen.
Kunt u een geneesmiddel niet verkrijgen via de reguliere groothandel? Wij zorgen voor de import, zodat u minder tijd kwijt bent aan het zoeken naar alternatieven.
Kennismaking
Mijn naam is Rutger Mulder, oprichter van Armuntis. Met ruim 12 jaar ervaring in de geneesmiddelenimport binnen de zorgsector, besloot ik in 2025 mijn kennis en expertise in te zetten om een bijdrage te leveren aan het oplossen van geneesmiddeltekorten.
Met Armuntis wil ik de gehele zorgketen – van fabrikant tot patiënt – ontzorgen. Niet alleen bij tekorten, maar ook bij het toegankelijk houden van zorg die steeds moeilijker beschikbaar wordt.
Heeft u te maken met een tekort waarbij wij kunnen helpen? Laat het ons weten via ons contactformulier.
Wat wij bieden
Naast onze expertise in de import van geneesmiddelen beschikken wij over uitgebreide kennis van de apotheekmarkt. Wij ondersteunen uw apotheek actief in het vinden van oplossingen voor geneesmiddeltekorten. U ontvangt gerichte alternatieven, zodat u minder tijd hoeft te besteden aan het zoeken naar passende oplossingen. Daarnaast hebben we een breed assortiment waaruit u gemakkelijk een alternatief kunt vinden.
De voordelen
- Bestellen via uw AIS of eenvoudig online via ons portaal
- Eigen voorraad en snelle levering
- Alle documentatie direct inzichtelijk via ons portaal
- Gegarandeerde GDP kwaliteit
- Wereldwijde importmogelijkheden
- Artikelen zichtbaar in de z-index
Meld een tekort
Wij nemen zo snel mogelijk contact met u op.
Registreer uw apotheek
Profiteer direct van ons volledige assortiment.

Waarom geneesmiddeltekorten?
Geneesmiddeltekorten zijn onder te verdelen in tijdelijke en definitieve tekorten. Bij een tijdelijk tekort is het geneesmiddel wel geregistreerd in Nederland, maar tijdelijk niet leverbaar door de vergunninghouder. Bij een definitief tekort is het geneesmiddel niet (meer) geregistreerd in Nederland.
Tijdelijke tekorten
Tijdelijke geneesmiddeltekorten betreffen vrijwel altijd generieke geneesmiddelen. Wanneer een geneesmiddel nog onder patent valt, heeft de fabrikant als het ware een monopoliepositie. De prijs van een geneesmiddel ligt tijdens de patentperiode dan ook aanzienlijk hoger dan wanneer er generieke alternatieven beschikbaar zijn. Omdat er slechts één aanbieder is en de prijs relatief hoog ligt, is het voor de fabrikant van groot belang dat het geneesmiddel continu leverbaar blijft.
Na afloop van de patentperiode komen er meerdere aanbieders van hetzelfde middel op de markt, deze moeten met elkaar concurreren om marktaandeel. Bij aanbestedingen en prijsonderhandelingen is prijs een doorslaggevende factor, waardoor generieke leveranciers zo efficiënt mogelijk moeten inkopen. Vaak produceren zij in grote fabrieken die meerdere landen bedienen. Nederland is op wereldschaal een relatief kleine afzetmarkt. Door de lage prijzen als gevolg van onder meer het WGP-beleid, aanbestedingen en prijsdruk, hebben wij een lage prioriteit in de internationale distributie.
Daarnaast baseren generieke leveranciers hun productie op verwachte marktaandelen. Als hierin onverwachte verschuivingen ontstaan, kunnen zij deze vaak niet opvangen. De lage marges maken het namelijk financieel onaantrekkelijk om extra voorraad aan te houden, vanwege de hogere financieringskosten en het risico op onverkoopbare overschotten.
Voor dit soort tijdelijke tekorten bieden import via tijdelijke ontheffingen voor kritische geneesmiddelen een oplossing. In situaties waarin zo’n ontheffing (nog) niet is afgegeven, kan levering op artsenverklaring uitkomst bieden.
Definitieve tekorten
Wanneer een geneesmiddel helemaal niet (meer) beschikbaar is, spreekt men van een definitief tekort. Dit kan verschillende oorzaken hebben. Soms is het geneesmiddel nog niet in Nederland beschikbaar omdat de vergunningsaanvraag nog in behandeling is. In andere gevallen kan het zijn dat er inmiddels alternatieve geneesmiddelen op de markt zijn gekomen met een betere werking of minder bijwerkingen. Ook komt het voor dat een middel slechts bedoeld is voor een zeer kleine patiëntengroep, waardoor het voor de vergunninghouder niet rendabel is om het geneesmiddel in Nederland beschikbaar te stellen.
Voor dit type tekorten kan levering op artsenverklaring en generieke toestemmingen op artsenverklaring een uitkomst bieden. Via deze weg is levering van een geïmporteerd geneesmiddel toch mogelijk en kan de patiënt toch de juiste zorg ontvangen.
Geneesmiddeltekorten en import
Welke vormen van import bij tekorten zijn er?
- Tijdelijk afwijkende verpakking (TAV)
- Parallel import
- Import met tijdelijke toestemming (3.17a)
- Tijdelijk niet handhaven op aanwijzing van VWS
- Generieke toestemming op artsenverklaring
- Artsenverklaring
Substitutie met geregistreerde alternatieven
Voor geneesmiddeltekorten bestaan meerdere oplossingsrichtingen. Het importeren van geneesmiddelen die niet in Nederland geregistreerd zijn, is vaak het laatste redmiddel. Wanneer een geneesmiddel niet leverbaar is, wordt eerst gekeken naar een alternatief met dezelfde werkzame stof — eventueel in een andere sterkte of van een ander merk — het zogenoemde farmaceutisch alternatief. Indien dit niet beschikbaar of passend is, kan men uitwijken naar een middel met een andere werkzame stof maar dat wel geschikt is voor dezelfde indicatie: een therapeutisch alternatief. Zowel farmaceutische als therapeutische alternatieven zijn echter lang niet altijd wenselijk voor de patiënt. Ze kunnen gepaard gaan met zwaardere bijwerkingen of een minder effectieve werking bij de betreffende aandoening.
Tijdelijk afwijkende verpakking
Wanneer een geregistreerd geneesmiddel niet leverbaar is, is de fabrikant in Nederland verplicht hiervan melding te maken. In overleg met de betrokken instanties wordt vervolgens gezocht naar passende oplossingen. Eén van deze oplossingen is het op de markt brengen van een tijdelijk afwijkende verpakking. Dit houdt in dat de fabrikant in een ander land – bijvoorbeeld Frankrijk – nog wel over voorraad beschikt, maar dan in een buitenlandse verpakking zonder Nederlandse tekst. Met toestemming van de instanties mag de fabrikant deze verpakking voorzien van een Nederlandstalig label en bijsluiter, waarna het product tijdelijk op de Nederlandse markt beschikbaar kan worden gesteld.
Deze oplossing kent echter beperkingen. Het herverpakken moet plaatsvinden onder GMP-omstandigheden, vereist officiële goedkeuring en kost tijd. Daardoor is het niet altijd geschikt bij acute tekorten. Bovendien zijn niet alle fabrikanten uitgerust om dit soort uitzonderlijke trajecten snel en efficiënt uit te voeren. Een bijkomende voorwaarde is dat er daadwerkelijk voldoende voorraad beschikbaar moet zijn van exact hetzelfde geneesmiddel, geproduceerd door exact dezelfde fabrikant. Alleen dan kan deze route worden ingezet.
Parallel import
Parallelimport betreft in vrijwel alle gevallen het spécialité-geneesmiddel: het oorspronkelijke merkgeneesmiddel waarvoor de fabrikant tijdens de patentperiode exclusieve productierechten heeft. Tijdens deze periode heeft de fabrikant een monopolie op de werkzame stof en is daarmee de enige producent. Omdat de fabrikant de productie en prijs nagenoeg volledig controleert, komen tekorten op spécialité-geneesmiddelen tijdens het patent zelden voor.
Parallelimport is oorspronkelijk ontstaan de prijs en daarmee de marge van het merkgeneesmiddel aantrekkelijker te maken voor de markt. Vrijwel alle parallelregistraties hebben betrekking op merkgeneesmiddelen, niet op generieken. Waar generieke fabrikanten na het verlopen van het patent bijdragen aan prijsdruk, doet parallelimport dit tijdens de patentperiode.
Binnen Europa bestaan grote prijsverschillen voor geneesmiddelen, onder andere door nationale wetgeving, prijsonderhandelingen en verschillen in zorgstelsels. Een parallelimporteur importeert exact hetzelfde geneesmiddel uit een ander (goedkoper) EU-land, verpakt dit om conform de lokale taal en regelgeving, en biedt het aan tegen een concurrerende prijs.
Bij tekorten – die vrijwel altijd generieke geneesmiddelen betreffen – kan parallelimport soms alsnog een rol spelen, mits een importeur al een geldige registratie heeft van het oorspronkelijke spécialité-geneesmiddel. Een nieuwe parallelregistratie is in acute situaties vrijwel nooit een oplossing, aangezien het proces maanden kan duren. Bovendien is na patentverval de prijs gedaald en het marktaandeel van het spécialité sterk afgenomen, waardoor beschikbaarheid voor import vaak beperkt is.
Kortom, parallelimport kan in sommige gevallen een bijdrage leveren aan het oplossen van geneesmiddeltekorten, maar alleen onder specifieke omstandigheden en in beperkte mate.
Import met tijdelijke toestemming (3.17a)
Omdat geneesmiddeltekorten niet altijd effectief kunnen worden opgelost met een in Nederland geregistreerd alternatief, TAV (tijdelijk afwijkende verpakking) of parallelimport, is er aanvullende wetgeving in het leven geroepen. Artikel 3.17 van de Geneesmiddelenwet biedt de mogelijkheid om in tijden van kritieke tekorten tijdelijk niet-geregistreerde geneesmiddelen te importeren.
Deze ontheffing mag uitsluitend worden gebruikt voor geneesmiddelen die als kritisch zijn aangemerkt en kan alleen worden verleend door de Inspectie Gezondheidszorg en Jeugd (IGJ). Import is uitsluitend toegestaan vanuit landen met vergelijkbare kwaliteitsstandaarden, zoals EU-lidstaten, MRA-landen en het Verenigd Koninkrijk. Dankzij deze regeling kan gebruik worden gemaakt van (bijna) wereldwijde voorraden van kritieke geneesmiddelen, terwijl de kwaliteit gewaarborgd blijft.
Eind 2024 heeft de Raad van State geoordeeld dat de IGJ deze ontheffingen formeel niet mag verlenen, omdat de huidige Geneesmiddelenwet vereist dat vooraf altijd een individueel verzoek bij de IGJ wordt ingediend voor levering van niet-geregistreerde geneesmiddelen. De wet zal daarom moeten worden aangepast om deze bredere bevoegdheid aan de IGJ te geven. Inmiddels wordt hieraan gewerkt.
Als tijdelijke maatregel heeft de minister van Volksgezondheid besloten om tijdens kritieke tekorten niet handhavend op te treden tegen overtredingen van de wet bij het importeren van niet-geregistreerde geneesmiddelen. Dit zorgt ervoor dat patiënten in noodsituaties toch toegang kunnen krijgen tot de benodigde medicatie, zolang aan de overige kwaliteits- en veiligheidsvoorwaarden wordt voldaan.
Tijdelijk niet handhaven op aanwijzing van VWS
Sinds eind 2024 mag de IGJ geen algemene ontheffingen meer verlenen voor de import van niet-geregistreerde geneesmiddelen. Als reactie hierop heeft de minister van Volksgezondheid een gedoogbeleid ingevoerd om tijdens kritieke tekorten toch in oplossingen te kunnen voorzien.
Onder dit beleid publiceert de IGJ een lijst van geneesmiddelen waarvoor zij tijdelijk niet handhavend optreedt bij overtredingen met betrekking tot de import van niet-geregistreerde geneesmiddelen. Net als bij de eerdere tijdelijke ontheffingen op grond van artikel 3.17a van de Geneesmiddelenwet, geldt ook voor dit gedoogbeleid een beperkt tijdsbestek. Buiten deze termijn hervat de IGJ haar handhaving.
Met dit gedoogbeleid is er een werkbaar alternatief gecreëerd voor de zorgsector. De systematiek is vrijwel gelijk aan die van een officiële IGJ-ontheffing: import is onder voorwaarden toegestaan, en de beschikbaarheid van geneesmiddelen wordt vergroot zonder in te leveren op veiligheid of kwaliteit. Het maakt voor alle partijen in de zorg geneesmiddelen beter beschikbaar.
Generieke toestemming op artsenverklaring
Naast import op basis van tijdelijke ontheffing en het gedoogbeleid, beschikt de IGJ ook over de mogelijkheid om een generieke toestemming te verlenen voor de aflevering van niet-geregistreerde geneesmiddelen op artsenverklaring.
De eerder genoemde oplossingen zijn uitsluitend van toepassing op tijdelijke tekorten, die – hoewel soms langdurig – van tijdelijke aard zijn. Echter, er zijn ook geneesmiddelen die definitief niet (meer) beschikbaar zijn in Nederland omdat zij niet (meer) geregistreerd zijn. In dergelijke gevallen is er dus geen sprake van een tijdelijk tekort maar van een definitief tekort.
Voor sommige van deze geneesmiddelen ontvangt de IGJ regelmatig aanvragen van apotheken om deze op basis van een artsenverklaring te mogen afleveren. Hierbij heeft een arts beoordeeld dat er voor de betreffende patiënt geen geschikt geregistreerd geneesmiddel op de markt is, en dat behandeling met een niet-geregistreerd geneesmiddel noodzakelijk is.
Om dit proces te stroomlijnen, heeft de IGJ in haar aanvraagformulier voor levering met toestemming op artsenverklaring een aantal veelvoorkomende geneesmiddelen opgenomen waarvoor eerder toestemming is verleend. Dit vergemakkelijkt de procedure voor zowel apotheken als importeurs.
Hoewel er nog steeds sprake is van administratieve verplichtingen – wat zowel voor de apotheek als de importeur extra werk met zich meebrengt – is het traject voor veelvoorkomende aanvragen inmiddels sneller en efficiënter ingericht, wat de beschikbaarheid van noodzakelijke geneesmiddelen voor de patiënt ten goede komt.
Artsenverklaring
Indien het geneesmiddel waarmee de patiënt behandeld moet worden niet is opgenomen in het formulier van de IGJ – en dus niet regelmatig wordt aangevraagd – dient de apotheek per patiënt afzonderlijk toestemming aan te vragen voor aflevering op basis van een artsenverklaring.
Deze werkwijze biedt een belangrijke uitkomst bij ziektebeelden waarvoor in Nederland (nog) geen geregistreerde behandeling beschikbaar is. Samen met de artsenverklaring kan dan een verzoek tot levering worden ingediend bij de IGJ.
Let op: aan deze procedure zijn verplichtingen verbonden voor zowel de apotheek als de importeur. De specifieke voorwaarden en vereisten zijn terug te vinden op de website van de IGJ (Inspectie Gezondheidszorg en Jeugd).
Armuntis
Heeft u hulp nodig bij de import van niet geregistreerde geneesmiddelen of heeft u last van een tekort bij geneesmiddelen, wij helpen u verder. Neem contact met ons op en wij zullen samen met u naar de juiste oplossing zoeken.


